精彩讲座
绝经后子宫出血的评估一定要做宫腔镜吗?超声检查评估的价值何在?何时需进一步检查,门诊子宫内膜取样或诊刮术有哪些局限性,如何能更好的避免这类创伤性检查?对于非预期的绝经相关子宫出血管理比较复杂,分类管理是个很好的策略。

01

在早期观察性研究中,Steve Goldstein 于1990年首次报道了超声内膜为7mm,被认为是最薄内膜的子宫内膜癌1。此后相继有很多学者参与到子宫内膜厚度与子宫内膜癌相关性的研究中。以Steve Goldstein 教授多年的临床经验,最常见的增厚的子宫内膜常出现在子宫内膜息肉和单纯性增生中。那么,经阴道超声是否能预测哪些患者缺乏足够的内膜组织,可以避免进一步行子宫内膜诊刮或活检?
一.盆腔经阴道超声检查评估子宫内膜
一项由Karisson 等人参与的早期观察性研究即著名的“Nordic Trial ”,发现1168例超声显示子宫内膜厚度≤4mm的绝经后子宫出血妇女,病理确诊无子宫内膜癌。另一项由意大利的Ferrazzi 等人进行的研究,报道了930例超声显示子宫内膜厚度≤4mm的绝经后子宫出血妇女,子宫内膜癌病例数为2例;若以≤5mm为临界值,则子宫内膜癌病例数为4例。此后相继报道一些有关绝经后子宫出血妇女的子宫内膜厚度与子宫内膜癌的研究。一项文献总结表明:经阴道超声显示子宫内膜厚度≤4mm的绝经后子宫出血妇女中,每917例有1例子宫内膜癌(图1)。如此低的子宫内膜癌发生率,是否有必要行子宫内膜活检?
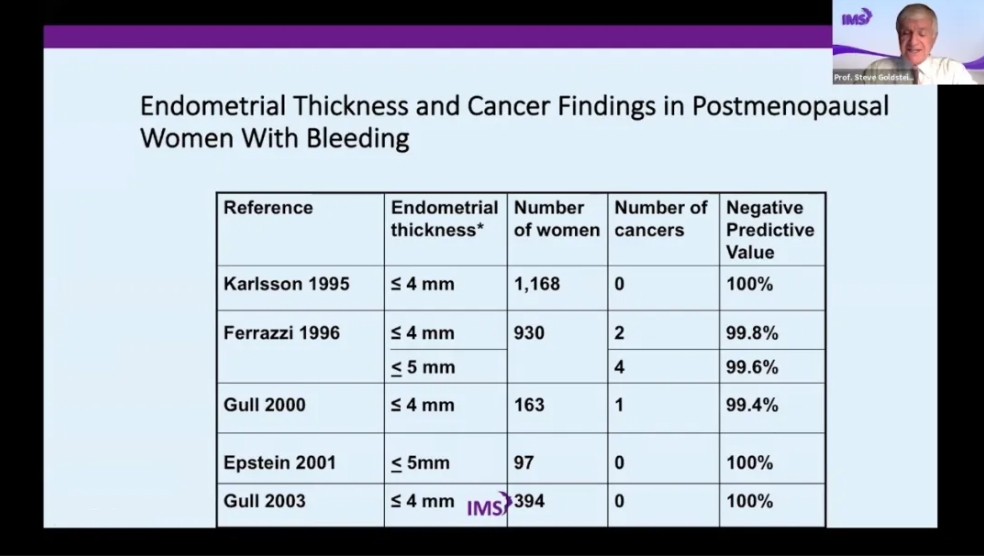
图一
一项由Elsandabesee D等学者于2005年发表的研究指出,经阴道超声子宫内膜厚度≤4mm预测子宫内膜癌的假阴性率远低于子宫内膜活检,如果在超声提示子宫内膜厚度<5mm的绝经后子宫出血的妇女中行子宫内膜活检,仅82%的患者成功进行了此项操作,而在进行该操作的患者中仅27%取到了足够的组织行病理诊断2。所以,2009年美国妇产科医师学会(American College of Obstetricians and Gynecologists, ACOG)的立场是:“对于绝经后子宫出血妇女,经阴道超声显示子宫内膜厚度≤4mm, 则不需要进行子宫内膜取样”。Wong等人于2016年再次以3mm, 4mm, 5mm 为临界值进行研究,发现以4mm为临界值,预测子宫内膜癌的阴性预测值为99.6%。综合此项最新研究,ACOG通过一项文献总结表明观点:如果以3mm为临界值,发生子宫内膜癌的机会是每383例患者有1例子宫内膜癌;如果以4mm为临界值,发生子宫内膜癌的机会是每339例有1例;如果以5mm为临界值,发生子宫内膜癌的机会为每239例有1例。(图二)。

图二
因此,对于无风险因素的绝经后阴道出血妇女,盆腔经阴道超声评估子宫内膜采用≤4mm为临界值,低于该值则不需要进一步评估。但是,对于存在肥胖、高血压、糖尿病、有多囊卵巢综合征病史等高危因素的妇女或反复子宫出血的妇女,尽管最初评估子宫内膜很薄,进一步的评估则是合理的。
用最高频率的传感器能产生足够的穿透力。
测量尽量放大到足够大使内膜回声清晰可见。
在子宫的长轴面得到多个图像,测量从一侧基底层到对侧基底层的前后距离。
测量应在长轴视野的内膜最厚点垂直测量。
子宫腺肌症
并存子宫肌瘤
宫颈与子宫长轴垂直
显著的肥胖
子宫手术史
2012ACOG实践指南指出妇科门诊中1/3的患者为异常子宫出血,其占围绝经期及绝经后妇科就诊咨询的70%。40岁到绝经的异常子宫出血可能是无排卵性出血,属于正常生理性的卵巢功能下降。绝经相关子宫出血也可能是子宫内膜癌、增生、内膜萎缩或子宫肌瘤。为什么包括了围绝经期出血,因为绝经后出血很难定义,绝经本身就是一个回顾性的诊断且绝经过渡期晚期卵巢功能的不确定性使绝经后出血的诊断更加困难,尽管如此,但诊断子宫内膜癌需要反复评估检查直至确诊。ACOG颁布的指南指出任何大于40岁怀疑存在异常子宫出血的妇女有指征行子宫内膜评估来排除子宫内膜癌。
2019年美国癌症协会指出子宫内膜癌是发病率最高的妇科恶性肿瘤。因子宫内膜癌早期常出现阴道出血的征象,易早期发现,所以大部分并不是致死性的。绝经后出血子宫内膜癌的发生率为1%-14%。大部分女性绝经后出血事实上是阴道或子宫内膜的萎缩性出血。
二.子宫内膜取样
子宫内膜取样器由精巧、便宜、一次性的外鞘包裹活塞内芯组成,主要通过产生负压将子宫内膜吸入。市场上比较成功的内膜取样装置品牌是Pipelle。Pipelle 最早于1984年由Cornier 在文章中描述,1991年Tom Stovall 报道40例确诊为子宫内膜癌的患者,在子宫切除术前曾行Pipelle取样,发现39例取样与术后病理子宫内膜癌相符,因此认为准确率达97.5%,自此Pipelle取样被广泛宣传。1994年Rodrigue报道通过Pipelle内膜取样仅能取到4%的子宫内膜腔面积,与术后诊断符合率仅有84%。但Guido R.等学者研究65例确诊为子宫内膜癌的患者,在子宫切除术前曾于麻醉下行Pipelle取样,结果发现Pipelle取样活检使11例患者漏诊,占比16.9%。该11例被漏诊子宫内膜癌患者行子宫标本剖探,3例癌灶小于5%内膜区,4例癌灶存在于6%-25%内膜区,4例癌灶存在于26%-50%内膜区。同时发现,此11例患者中5例肿瘤存在于息肉中。Guido的结论是:Pipelle适合于均匀性子宫内膜的取样。相继有学者报道盲性子宫内膜取样的假阴性率,此后像Pipelle这样的子宫内膜取样抽吸装置的可信性受到彻底的颠覆(图三)。Steve Goldstein认为:除非确认子宫内膜整体均匀并非局灶性的,否则不适合行盲性子宫内膜活检。

图三
✦评估异常子宫出血的患者时,门诊子宫内膜活检是组织取样的一线操作(比如,门诊超声评估不可行时,即可行内膜活检取样评估)。
✦当子宫内膜是均匀性增厚且获得足够的组织标本时,子宫内膜活检诊断子宫内膜癌有高的整体诊断价值。
✦如果子宫内膜癌灶占据的内膜腔表面范围<50%,癌灶可能被盲性活检漏诊。
✦在排除疾病方面,阳性结果比阴性结果更准确。
✦检测结果仅在显示子宫内膜癌或不典型增生才是最终结果。
✦现有监测标准证实阴性的盲性活检不是终止检查点。临床医生仍可从活检开始诊治,除非子宫内膜活检是恶性的或复杂性不典型增生,否则子宫内膜评估是不完整的。
三.子宫声学造影
子宫声学造影又称盐水灌注超声造影,是用无菌性生理盐水注入子宫内膜腔后行经阴道超声检查。液体可增强声音的传播,该技术可对宫腔结构进行仔细的评估以发现微小病变,可能对于影像科医师有一定难度,但对妇产科医生来讲却很简单。作为经阴道超声的子设备,主要用于:
1)当子宫内膜不是足够的薄(比如:子宫内膜较厚)。
2)因医学技术上原因子宫内膜不是足够的清晰可见时,包括存在子宫肌瘤、子宫腺肌症、宫颈与子宫长轴垂直等。

异常子宫出血的主要的影像学检查是经阴道超声,如果经阴道超声不足以很好的评估子宫内膜或需要进一步评估内膜腔,则推荐子宫声学造影或宫腔镜。
四.总结
1. 行子宫内膜厚度测量时,经阴道超声对薄的子宫内膜有高的阴性预测价值。
2. 超声评估子宫内膜≤4mm的大部分绝经后子宫出血妇女,有很低的恶性风险,不需要内膜取样。
3. 如果经阴道超声评估不足以排除异常,盐水灌注超声造影或宫腔镜能够区分整体及局灶病变,并能够合适的分类(整体病灶盲性活检,局部病灶则直视)。
4. 进一步理解经阴道超声的可信性,必要时行子宫声学造影或宫腔镜。认识盲性内膜活检的局限性,进一步理解绝经后子宫出血行经阴道超声及子宫声学造影的作用及重要性。

对于非预期绝经相关子宫出血的管理比较复杂,将按照以下三个议题为大家介绍,相信对临床问题的解决更有帮助。首先,怎样管理已经确定病理组织学类型的绝经后出血,不同的诊断可能需要不同的管理,所以需要理解不同病理组织学类型的术语及其意义,这将帮助临床医生做出更好的决策。然后,强调绝经后出血子宫内膜息肉的管理,目前子宫内膜息肉没有一个完整清晰的治疗方向,希望通过讲述至少在从哪里入手上有一个更好的思路。最后,绝经激素治疗中非预期出血的管理。
一.子宫内膜增生
过去认为有四种类型的子宫内膜异常,包括单纯性增生,复杂性增生,不典型增生以及子宫内膜癌。2014年WHO更改了子宫内膜增生分类系统,将其简化为两类:不伴非典型的增生和非典型增生(也称为子宫内膜上皮内瘤变)。曾经认为这是一个连续体,进展沿着连续体发生,事实上这是两个完全不同的事件。目前认为不伴不典型的增生基因稳定,并未发生基因改变,不趋向于进展,所以极少会进展为子宫内膜癌,可能5年只有1%-3%,正因如此,管理方面也是保守性的3。在一些实例中,保守性管理有可能包括不进行任何治疗,虽然该做法可能不被认可,但或许是不伴不典型增生管理的一个研究阶段。
1.子宫内膜不伴非典型增生
生活方式的调整很重要,最重要的是超重及肥胖与子宫内膜癌患病风险相关,BMI超过30kg/m2是正常BMI者的4倍。所以生活方式的调整特别是减重,是管理任何一种异常子宫内膜的基石。
左炔诺孕酮宫内缓释系统(Levonorgestrel-releasing intrauterine system LNG-IUS 52mg)是治疗不伴不典型增生的一线治疗方案(A级推荐)。它具有更高的疾病转归率,很少副反应事件,但是不规则出血的情况容易发生,受到多个指南的一致推荐,尤其是获得英国皇家妇产科医师学会(Royal College of Obstetricians and Gynaecologists, RCOG)和英国妇科内镜协会(British Society for Gynaecological Endoscopy, BSGE)联合指南的推荐4。该指南认为如果用口服孕激素应连续不间断用药,推荐醋酸甲羟孕酮10-20mg/日或炔诺酮10-15mg/日(B级推荐)。不应该周期性孕激素治疗,它并不比连续用孕激素及LNG-IUS有效(A级推荐)。仅有诊断和治疗是不够的,推荐持续的内膜监测(C级推荐)。加拿大的指南中认为注射用甲羟孕酮,100mg, 每3个月一次肌肉注射,也是可接受的选择,有研究表明92%的转归率5。一些特殊情况下需考虑子宫双附件切除术。
✦随访监测中进展;
✦12月治疗未转归;
✦未连续治疗出现复发;
✦不适合药物治疗。
2.子宫内膜不典型增生
子宫内膜不典型增生的基因及分子生物的改变有致癌风险,基因改变与癌相似,被认为是I型子宫内膜癌的前期病变。子宫内膜不典型增生多久会进展为癌呢?来自丹麦的数据库分析6,超过60%的患者在组织学病理诊断为不典型增生或上皮内瘤变时,经子宫切除手术证实已是子宫内膜癌。这是文献中报道比较高的数据,大部分的文献报道是30%-35%,无论如何都是比较高的发生率,因此推荐绝经妇女行全子宫双附件手术,首先考虑微创手术,经腹手术主要限于不适合微创的患者3。
✦绝经前女性希望保留生育力;
✦绝经后妇女医学上不适合手术。
3.小结
子宫内膜不伴不典型的增生,不太可能进展,治疗方面持续的孕激素管理,最少治疗6个月,注意监测。绝经后妇女在监测中发现进展、没有转归、治疗缺乏依从性或治疗后再复发要考虑手术。子宫内膜不典型增生(或者子宫内膜上皮内瘤变)是子宫内膜癌的前期病变,高达60%的妇女事实上已经发展为子宫内膜癌,推荐微创子宫双附件切除手术,特殊情况下再考虑药物管理。
二.子宫内膜息肉
子宫内膜息肉是宫腔局部内膜基底层增生形成的肿瘤,大约1/3绝经后妇女有子宫内膜息肉,可能并不伴出血症状;有趣的是子宫内膜息肉增加了雌激素受体,减少或没有孕激素受体,所以用孕激素并不能达到治疗效果7。怎样做出临床决策,什么时候需要切除息肉?一篇很好的综述8,Ferrazzi等人纳入约2000名绝经后妇女通过妇科超声或子宫声学造影诊断子宫内膜息肉,进行了宫腔镜直视下息肉摘除,结果为:绝经后妇女息肉伴有出血,息肉术后病理诊断为不典型增生者占2.2%,癌的发生率为1.0%;而绝经后妇女仅有息肉,不典型增生的发生率为1.2%,癌的发生率为0.1%。基于这样的证据,2012年美国妇科腹腔镜医师协会(American Association of Gynecologic Laparoscopists, AAGL)实践指南9推荐手术切除所有有症状的息肉,宫腔镜直视下从蒂的根部切除完整息肉。即无症状的息肉无需手术,但该指南未提到对息肉周围组织的取样,且缺乏不典型息肉的管理共识。

1.绝经后妇女息肉伴子宫出血症状则增加了增生和恶性的风险。
2.绝经后妇女息肉伴子宫出血症状应在直视下从蒂根部完整息肉摘除,同时息肉周围行内膜取样。
3.管理应该根据息肉组织病理分类(低证据水平)或根据息肉周围内膜组织增生病理分类(低证据水平,D级)。虽为低证据水平,其是目前可用到的最好的管理推荐。
三.绝经激素治疗中非预期出血的管理
非预期的子宫出血是中止绝经激素治疗的主要原因,占到所有中止原因的1/3。目前确切机制并不明确,可能和一些孕激素导致内膜微血管的改变有关。激素剂量不合适可能更容易出血。目前除了建议适当的检查,包括体格检查排除非子宫原因的出血(注意排除宫颈出血,外阴阴道肿瘤出血等),并没有绝经激素治疗中子宫出血的管理指南。复习文献缺乏管理共识,很少有高质量证据的干预措施。
1.微粒化黄体酮-内膜保护剂
一项来自法国历时8年,纳入80000名妇女的E3N研究显示应用雌激素和微粒化黄体酮增加子宫内膜癌的风险,而事实上该风险更常见于无对抗的雌激素应用,该研究缺乏应用微粒化黄体酮的剂量、方式(周期性或连续性)及依从性的相关数据13,且未对经皮雌激素联合口服微粒化黄体酮进行足够关注14。另一项最近的研究则证明口服17-β雌二醇1mg联合100mg微粒化黄体酮具有子宫内膜安全性15。
关于微粒化黄体酮对子宫内膜的保护,Stute学者于2016年发表在Climacteric杂志上的一篇综述针对子宫内膜保护总结如下结论16:
✦每个月口服12-14天200mg的微粒化黄体酮具有内膜保护作用。
✦每个月10天45mg经阴道微粒化黄体酮或者隔天100mg。
✦经皮孕激素并不能提供足够的内膜保护作用。
✦目前认为雌孕激素连续联合应用时微粒化黄体酮减至100mg/日是可行的(始初为200mg/日)。如果选择超低剂量的雌激素治疗会出现闭经。基于这些证据,雌孕激素连续联合方案口服17-β雌二醇1mg联合100mg微粒化黄体酮可行。

2.绝经激素治疗方案
最近的一篇系统综述17,比较总结了雌孕激素连续联合治疗(不包括替勃龙和组织选择性雌激素复合物(TSEC))在北美和欧洲的应用,主要是调查从1周期到12/13周期的累积闭经周期、闭经率(12/13周期)、因非预期子宫出血中止治疗情况。总结出如下结论:
a. 雌孕激素连续联合治疗的最初6个月发生非预期子宫出血率最高,随着时间延长出血情况改善。
b. 口服激素治疗比经皮激素治疗能更好的控制出血。(该研究的局限性是经皮激素是固定剂量的制剂且包括有限的孕激素选择。应注意黄体酮并不经皮吸收,但合成孕激素能用于经皮吸收)。
c. 每天口服17-β雌二醇(E2)1mg联合100mg微粒化黄体酮(MP)比包含合成孕激素的药物有更好的出血改善情况(非直接比较研究结论)。炔雌醇(EE,ethinyl estrodiol)联合醋酸炔诺酮(NETA, norethisterone)也可以使用。
d. 更易出血的情况还出现在低剂量药物,同时发现离最后一次月经时间越远越不容易出血。
一项历时两年的临床试验研究18证明结合雌激素(conjugated estrogen, CE)0.45mg联合巴多昔芬(bazedoxifene acetate, BZA)20mg方案即TSEC方案,作为内膜保护剂,其出血模式在闭经和累积闭经方面与安慰剂相似,一年后有很高的闭经率。因乳房不适或出血症状,从其他绝经激素治疗方案转为TSEC方案后有97%的患者症状得到解决。直接比较TSEC方案与CE 0.45mg/MPA 1.5mg方案,发现后者在前六个月有更高的出血率,随着时间的推进逐渐好转,但是1年后仍有8.81%存在不规则出血症状。
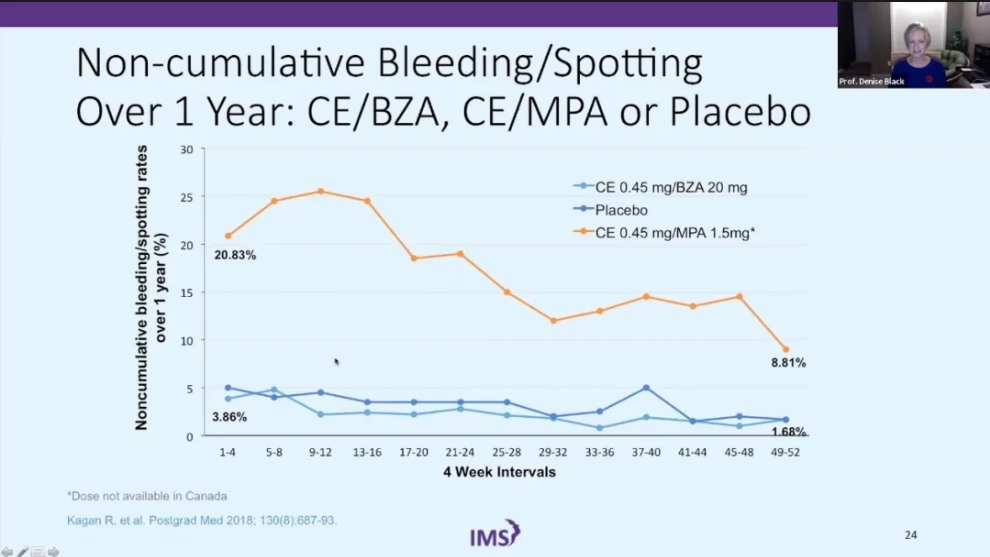
一项研究19显示,平均年龄为54岁且距离末次月经平均4.5年的绝经后妇女口服2.5mg替勃龙,持续一年时非预期的子宫出血率为10%。与最近另一项研究20口服17-β雌二醇1mg联合100mg微粒化黄体酮的出血率相似。
3.小结
✦目前很少有关于绝经激素治疗中非预期子宫出血相关管理的有科学依据的指南。
✦目前所有主要的指南推荐,对连续联合治疗6个月后出现的非预期子宫出血进行检查。
✦有限的证据认为TSEC、替勃龙、E2 1mg/MP 100mg及EE/NETA有更好的出血模式。
✦一项研究推荐将治疗方案更改为TSEC方案可能改善大部分妇女的出血症状。
【参考文献】:
[1]. Goldstein SR, Nachtigall M, Snyder JR, et al. Am J Obstet Gynecol. 1990; 163:119-123.
[2]. EIsandabesee D, Greenwood P;J Obstet Gynecol. 2005; 25:32-4.
[3]. Guideline No.390—Classification and Management of Endometrial Hyperplasia. J Obstet Gynaecol Canada. 2019 ;41(12):1789-1800.
[4]. Management of Endometrial Hyperplasia: Green Top Guideline No.67, RCOG/BSGE Joint Guideline February 2016.
[5]. Nooh et al. Reprod Sci. 2016 April; 23(4):448-454.
[6]. Antonsen S et al. Gynecol Oncol. 2012;125:124-128.
[7]. Sheng K, Lyons SD. To treat or not to treat? An evidence based practice guide for the management of endometrial polyps. Climacteric. 2020,23(4):336-342.
[8].Ferrazzi et al. Am J Obstet Gynecol. 2009;200:235
[9].J Minim invasive Gynecol. 2012;19:3-10.
[10].DeRijk SR et al. Obstet Gynecol. 2016; 128:519-525.
[11].Elyashiv et al. Journal of Minimally Invasive Gynecology 2017;24:1200-1204.
[12].SOGC Guideline no.390. J Obstet Gynaecol Canada. 2019;41(12):1789-1800.
[13].Fournier A et al. Am J Epid 2014; 189:508-517.
[14].Pickar JH et al. Climacteric. DOI:10.1080/13697137.2020.1806816.
[15].Mirkin S et al. Menopause. 2020;27:410-417.
[16].Stute et al. Climacteric. 2016;19:316.
[17].Pickar JH et al. Clinacteric 2020 DOI 10.1080?136971322020.1806816.
[18].Kagan R, et al. Postgrad Med 2018; 130(8):687-93.
[19].Archer DF et al. J Clin Endocrinol Metab2007, 92:911-918
[20].Lobo RA et al. Obstet Gyneacol. 2018;132(1):161-170
